Você já deve ter lido ou escutado que do fósforo aplicado ao solo apenas 15 a 25% são aproveitados pelas plantas. E na transação comercial de fertilizantes você nota, ou mesmo nas recomendações de adubação, que as fórmulas de fertilizantes minerais apresentam o P em maior concentração do que o NK. Por exemplo, formulações como 05-30-10, 04-14-8, 08-24-12 e tantas outras. Por que isto, se dos três macronutrientes principais (NPK) absorvidos pelas plantas, o fósforo (P) é aproveitado em pequena quantidade? O fósforo é mais necessário no estágio inicial da planta promovendo o seu crescimento e a formação de um bom sistema
Assuntos técnicos sobre fertilidade do solo, análise do solo, interpretação análise do solo, adubação, calagem, culturas em geral, fertilidade do solo, meio ambiente e agricultura sustentável.
Mostrando postagens com marcador fosfatos naturais reativos. Mostrar todas as postagens
Mostrando postagens com marcador fosfatos naturais reativos. Mostrar todas as postagens
segunda-feira, 3 de maio de 2021
terça-feira, 29 de maio de 2012
Adubação de Pastagens com Fosfato Natural Reativo
Existem diferenças acentuadas entre os solos brasileiros destinados à exploração de pastagens. A baixa fertilidade dos solos é a característica predominante. Isto acarreta problemas sérios quando se deseja obter pastagens de qualidade. Sem melhoria da fertilidade é impossível conseguir bons resultados no manejo das pastagens, para garantir alimento aos animais que traduzirão em produção de carne e leite. As plantas forrageiras possuem um grupo muito grande de espécies, com ciclos anual, bienal ou
terça-feira, 4 de outubro de 2011
Garantia do P2O5 no Uso dos Fosfatos Naturais
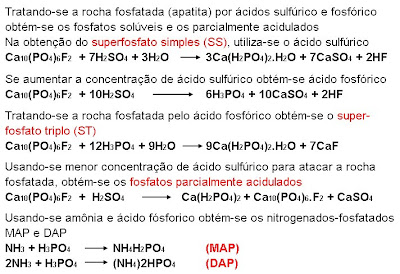
 Na postagem de 29 de setembro deste ano, sob o título "O que Diferencia os Fosfatos Naturais Reativos", abordamos sobre os fosfatos naturais apatíticos, de baixa solubilidade e que necessitam do ataque de ácidos ou do calor para solubilizar o seu fósforo, transformando-os nos chamados solúveis em água ou nos termofosfatos. Ao lado destes, os fosfatos naturais de origem sedimentar que podem ser aplicados diretamente na agricultura, pois não necessitam de nenhum tratamento químico ou térmico para tornar o seu fósforo aproveitável pelas plantas. E, entre eles, os fosfatos que são definidos como Fosfatos Naturais Reativos, pela sua
Na postagem de 29 de setembro deste ano, sob o título "O que Diferencia os Fosfatos Naturais Reativos", abordamos sobre os fosfatos naturais apatíticos, de baixa solubilidade e que necessitam do ataque de ácidos ou do calor para solubilizar o seu fósforo, transformando-os nos chamados solúveis em água ou nos termofosfatos. Ao lado destes, os fosfatos naturais de origem sedimentar que podem ser aplicados diretamente na agricultura, pois não necessitam de nenhum tratamento químico ou térmico para tornar o seu fósforo aproveitável pelas plantas. E, entre eles, os fosfatos que são definidos como Fosfatos Naturais Reativos, pela sua quinta-feira, 29 de setembro de 2011
O que Diferencia os Fosfatos Naturais Reativos
 Muitos questionam a eficiência dos fosfatos naturais e a solubilidade em determinados extratores. Os fosfatos naturais apresentam eficiência agronômica conforme a sua origem: uns são de origem apatítica, já cristalizados, duros, de baixa solubilidade tanto nos extratores ácido cítrico e/ou ácido fórmico, ambos na concentração de 2% e relação 1:100. Outros são de origem sedimentar, orgânicos, amorfos, que podem ser aplicados diretamente na agricultura, sem nenhum tratamento químico ou térmico.
Muitos questionam a eficiência dos fosfatos naturais e a solubilidade em determinados extratores. Os fosfatos naturais apresentam eficiência agronômica conforme a sua origem: uns são de origem apatítica, já cristalizados, duros, de baixa solubilidade tanto nos extratores ácido cítrico e/ou ácido fórmico, ambos na concentração de 2% e relação 1:100. Outros são de origem sedimentar, orgânicos, amorfos, que podem ser aplicados diretamente na agricultura, sem nenhum tratamento químico ou térmico. O que significa 1:100?
terça-feira, 2 de agosto de 2011
Qual o Melhor Fosfatado no Sistema Plantio Direto?
 Uma preocupação constante no meio técnico é a utilização de fosfatos naturais reativos nas áreas de plantio direto. Os fosfatos naturais reativos têm mostrado eficiência quando utilizados na forma pó. Já foram granulados, mas a eficiência agronômica vai depender de como foi feita esta granulação. O fosfato natural reativo, quando granulado, aplicado diretamente no solo, deve voltar rapidamente à forma de pó pelo contato com a umidade do solo. Nessas condições, a área de contato com os ácidos do solo, com as secreções ácidas liberadas pelas raízes das plantas, com os micro organismos do solo, é maior, o que aumenta a solubilização e liberação de fósforo disponível para as plantas. Como essa disponibilidade é
Uma preocupação constante no meio técnico é a utilização de fosfatos naturais reativos nas áreas de plantio direto. Os fosfatos naturais reativos têm mostrado eficiência quando utilizados na forma pó. Já foram granulados, mas a eficiência agronômica vai depender de como foi feita esta granulação. O fosfato natural reativo, quando granulado, aplicado diretamente no solo, deve voltar rapidamente à forma de pó pelo contato com a umidade do solo. Nessas condições, a área de contato com os ácidos do solo, com as secreções ácidas liberadas pelas raízes das plantas, com os micro organismos do solo, é maior, o que aumenta a solubilização e liberação de fósforo disponível para as plantas. Como essa disponibilidade é segunda-feira, 5 de julho de 2010
As Garantias Mínimas dos Fosfatos Naturais Reativos
O nosso leitor " forjengineer " publicou um comentário no blog sobre as garantias mínimas dos fosfatos naturais reativos que teriam sido alteradas pela Instrução Normativa n° 5. Disse o leitor que o P2O5 total, no mínimo, seria 27%, e que o P2O5 solúvel em ácido cítrico 2% 1:100 seria, no mínimo, 30% do teor total de fósforo garantido pelo indústria que o comercializa. Na nossa publicação, falamos de 28% de fósforo total e 9% de fósforo solúvel em ácido cítrico 2% 1:100. E o leitor forjengineer, atento à legislação brasileira de fertilizantes comentou esta diferença. Agradecemos ao mesmo por este comentário dando a possibilidade de atualizarmos o artigo.
terça-feira, 8 de junho de 2010
O Fósforo do Solo e a Eficiência Agronômica
Os solos brasileiros são ácidos e apresentam deficiências de P para as plantas. Embora exigido pelas culturas, em geral, em quantidades pequenas, o P é um fator limitante no aumento de produção das culturas. As plantas respondem muito bem à calagem, à fosfatagem e à manutenção dos níveis de P no solo, com aumento na produtividade. Entretanto, nos fertilizantes minerais granulados ou complexos, o nutriente P é expresso em percentagem maiores do que o N e K. Isto se deve ao fato de que apenas 15 a 25% do P aplicado ao solo´é absorvido pelas plantas, devido aos processos de fixação, retrogradação e outros já comentados em artigos anteriores (leia o artigo "clicando aqui").
O fósforo, no solo, encontra-se na fase sólida – orgânica e inorgânica, e na fase líquida – solução do solo. Nesta solução ele está presente como ânions H2PO4 e HPO4 e sua concentração é menor que 0,01 mg/dm³ ou 0,02 kg/ha. Esta é apenas uma pequena fração do fósforo total e é a forma solúvel que as plantas absorvem.
O fósforo, no solo, encontra-se na fase sólida – orgânica e inorgânica, e na fase líquida – solução do solo. Nesta solução ele está presente como ânions H2PO4 e HPO4 e sua concentração é menor que 0,01 mg/dm³ ou 0,02 kg/ha. Esta é apenas uma pequena fração do fósforo total e é a forma solúvel que as plantas absorvem.
terça-feira, 25 de maio de 2010
Solubilidade X Assimilabilidade das Fontes de Fósforo
Antigamente, uma corrente de agrônomos considerava que apenas o fósforo proveniente dos fosfatos solúveis em água seria aproveitado pela planta durante o seu desenvolvimento. O que não era solúvel em água não seria absorvido pela planta, e, consequentemente, não tinha nenhuma eficiência agronômica. Eles consideravam o solo como um mero suporte do vegetal para ele não cair. E parece que ainda existem os que defendem esta teoria. O solo não teria vida. Mas o que se sabe é que o solo é um meio dinâmico formado de estruturas coloidais, com a presença de ácidos fracos, de microorganismos, de CO2, de secreções ácidas liberadas pelas raízes, e que teriam a propriedade de solubilizar as fontes de fósforo liberando-o para as plantas.
Para uma melhor compreensão, abaixo temos uma ilustração do ciclo dos fosfatos solúveis em água.
Para uma melhor compreensão, abaixo temos uma ilustração do ciclo dos fosfatos solúveis em água.
terça-feira, 17 de novembro de 2009
O Fósforo no Solo e a Solubilidade dos Fosfatos
O fósforo, no solo, encontra-se na fase sólida – orgânica e inorgânica, e na fase líquida – solução do solo. Nesta solução ele está presente como ânions H2PO4 e HPO4 e sua concentração é menor que 0,01 mg/dm³. Esta é apenas uma pequena fração do fósforo total, e é a forma solúvel que as plantas absorvem. A absorção do fósforo pelas plantas se verifica sob a forma de ânions encontrados na solução do solo: o ânion H2PO4 predomina em solos ácidos e é chamado de ortofosfato primário; o ânion HPO4 em solos alcalinos e é chamado de ortofosfato secundário.
Tem sido adotada a expressão elementar de P para indicar os teores de fósforo ao invés de indicar o óxido P2O5. As plantas não utilizam nem o elemento puro e nem a forma de óxido (P2O5). É mais uma diferença acadêmica do que prática. Usam-se conversões como:
P2O5 x 0,437 = PTem sido adotada a expressão elementar de P para indicar os teores de fósforo ao invés de indicar o óxido P2O5. As plantas não utilizam nem o elemento puro e nem a forma de óxido (P2O5). É mais uma diferença acadêmica do que prática. Usam-se conversões como:
P x 2,29 = P2O5
Na dissociação, há formação de H+ que ocasiona um abaixamento do pH ao redor do grânulo de adubo.
Nos fertilizantes, o fósforo precisa combinar-se com hidrogênio, cálcio, oxigênio e outros elementos, porque as plantas não podem usá-lo, como os demais nutrientes, na sua forma elementar ou pura: na forma elementar, o fósforo queima-se quando em contato com o ar; o nitrogênio é um gás inerte, sem cor; o potássio se queima quando em contato com a água.
O teor de P2O5 em um fertilizante é expresso em porcentagem (%); é considerado prontamente disponível para as plantas em crescimento. Ele tem sido utilizado tradicionalmente para expressar o fósforo disponível. É chamado, também, óxido de fósforo, ou pentóxido de fósforo, ou anidrido fosfórico. Na realidade, o P2O5 nunca é encontrado como tal nos fertilizantes, mas o teor de fósforo contido neles tem sido expresso em P2O5%. É mais do ponto de vista histórico, tradição. Em ácidos onde não se verifica a presença de molécula de água ou, pelo contrário, se tem a presença de mais de uma molécula de água, ocorre o seguinte: 2 x H3PO4 = H6P2O8
3 x H2O = H6O3
H6P2O8 - H6O3 = P2O5
3 x H2O = H6O3
H6P2O8 - H6O3 = P2O5
No material de origem do solo, o P encontra-se na forma mineral, em maior parte, como fosfato de cálcio. Pela ação do intemperismo e de outros fatores que atuam na formação do solo, o fósforo é liberado para a solução do solo. Parte do fósforo é “adsorvida” pelos minerais secundários, e parte é “absorvida” e incorporada pelos microorganismos do solo; isto faz com que aumente a proporção de fósforo orgânico. Apesar do fósforo total do solo ser muito grande, apenas uma parte dele está em equilíbrio com o fósforo da solução do solo, e pode ser utilizada pelas plantas durante o seu desenvolvimento. Esta fração de P total é chamada “lábil” e é avaliada através de extratores na análise do solo.
Os solos são deficientes em fósforo devido ao processo de fixação; as plantas precisam de fósforo para produzir grãos e frutos; a exportação de P pelos vegetais é grande, correspondendo até 0,5% da massa seca.
Na maior parte dos solos, a solução do solo é muito baixa em concentração de nutrientes. Entretanto nesta solução fraca passam bilhões de íons por meio de complexos de troca e processos de difusão, com a finalidade de prover as raízes das plantas e a partir delas as folhas, grãos e frutos. Porém, muitos fatores afetam estes processos: disponibilidade de água; suprimento de oxigênio; atividade microbiana; temperatura do solo; e concentração de nutrientes.
O suprimento de oxigênio é um fator muito crítico, pois faltando o oxigênio a produção de energia pelas raízes é comprometida, e, com isto, a absorção de nutrientes é limitada. É o caso dos solos inundados ou com má drenagem.
Quanto à temperatura, solos frios reduzem o processo de absorção porque a produção de energia respiratória é prejudicada. Nestas condições ocorrem deficiências de fósforo e zinco.
A rocha fosfatada é a principal fonte de fósforo: são os fosfatos naturais. Estes podem ser ígneos ou sedimentares. Os ígneos, de origem vulcânica, são de baixa eficiência agronômica; sua reatividade, no solo, é quase zero; são de baixa solubilidade nos extratores ácidos fórmico e cítrico; são insolúveis em água. As rochas sedimentares, por sua vez, formadas por depósitos de animais marinhos, são brandas, estrutura frágil, com maior substituição isomórfica; são mais reativas, pois sua solubilidade em extratores ácidos é maior, apesar de serem insolúveis em água; sua eficiência agronômica é mais alta.
Na minha opinião, considero fosfatos naturais reativos para aplicação direta na agricultura: quando forem de origem sedimentar com alta brandura; apresentarem alto teor de fósforo solúvel no ácido fórmico 2% relação 1:100; terem mais de 55% do fósforo total solúvel no ácido fórmico 2% 1:100; aplicados em pó ou submetidos a uma granulação soft que os permitam, em contato com a umidade do solo, voltarem rapidamente à forma de pó.
Para que haja aproveitamento do P pelas plantas é preciso que ocorra a dissolução da apatita: Ca10(PO4)6 + H = Ca + HPO4
Então, a eficiência do fosfato natural será maior em solos ácidos, onde o Al não seja limitante, e em solos com P e Ca baixos. Em solos com alto teor de Ca e pH maior que 5,5 esta eficiência agronômica cairá porque a reação de dissolução não encontrará condições favoráveis. Por causa disto, a indústria de fertilizantes utiliza ácidos para romper a estrutura cristalina dos fosfatos naturais pouco reativos com a finalidade de aumentar a sua eficiência agronômica.
Nos fosfatos parcialmente acidulados, oriundos do tratamento da rocha fosfatada com uma menor quantidade de ácido sulfúrico, uma parte do fósforo torna-se solúvel em água e a outra continua insolúvel em água. A Legislação de Fertilizantes, no caso dos fosfatos parcialmente acidulados, obriga garantir o teor de P2O5 solúvel em citrato neutro de amônio (CNA) + água. Os teores de P2O5 solúvel em água e total somente quando são vendidos isoladamente. Nestes fosfatos, tem-se uma liberação imediata do fósforo (vindo da solubilização) e a outra parte permanece insolúvel.
O fósforo solúvel em água reage instantaneamente no solo liberando grandes quantidade de fósforo que são adsorvidos aos colóides do solo. O fornecimento de P às plantas dependerá da reatividade do fósforo e da capacidade do solo de fixá-lo. Por isto os fosfatos devem ser aplicados no momento da semeadura, pois a ligação com os colóides do solo torna-se muito forte com o passar do tempo; além disto, os fosfatos devem ser aplicados em grânulos e na linha de semeadura para diminuir a área de contato com os colóides inorgânicos e tornar menor a adsorção.
E os fosfatos naturais reativos quando aplicados diretamente no solo? Os fosfatos naturais reativos (falo somente em reativos), pelo contrário, devem aumentar a área de contato com os colóides do solo e devem ser aplicados a lanço e incorporados ao solo.
Lembre-se! Só haverá liberação de P : quando o solo fornecer H para a reação; quando o P e Ca da solução, que foram liberados pela dissolução, sejam consumidos.
sexta-feira, 29 de maio de 2009
Produtos orgânicos X fertilizantes minerais - Parte III
Os materiais orgânicos são divididos em quatro tipos:
1. Simples – são aqueles originados de plantas ou de animais. É o caso dos estercos de bovinos e suínos, camas de f rango, torta de mamona, vermicomposto, turfa, linhita, etc... O esterco fresco, que contém microorganismos causadores de doenças no homem, não é permitido o seu uso em culturas, em que a parte comestível pela população humana possa entrar em contato direto com ele. Para isto, ele deve ser “curtido”, processo que pode levar até 90 dias dependendo das condições climáticas. O esterco fresco, durante o curtimento, deve ficar protegido e ser evitado o escorrimento de água que levaria embora os nutrientes contido neles.
rango, torta de mamona, vermicomposto, turfa, linhita, etc... O esterco fresco, que contém microorganismos causadores de doenças no homem, não é permitido o seu uso em culturas, em que a parte comestível pela população humana possa entrar em contato direto com ele. Para isto, ele deve ser “curtido”, processo que pode levar até 90 dias dependendo das condições climáticas. O esterco fresco, durante o curtimento, deve ficar protegido e ser evitado o escorrimento de água que levaria embora os nutrientes contido neles.
2. Mistos – são originados da mistura de dois ou mais orgânicos simples;
3. Compostos – estes não são um orgânico natural. São obtidos por processos químicos, físico, físico-químicos ou biológicos. Podem ser, ainda, enriquecidos com nutrientes minerais. Formados por restos de vegetais e animais são obtidos por via aeróbica (presença de ar). Sua utilização é importante, pois melhora as condições físicas, químicas, físico-químicas e biológicas do solo favorecendo o enraízamento das plantas. Nos compostos se usa restos de vegetais, ricos em carbono (C), e de animais. O esterco é rico em nitrogênio (N). Isto é importante para estabelecer a relação C/N, que inicialmente deve ser 30/1. Devem-se usar mais resíduos vegetais ricos em carbono. O processo para formar o composto é distribuir camadas alternadas de restos vegetais e de animais. Cada camada vai sendo umedecida com água evitando-se o escorrimento para não haver perda de nutrientes. Pode ser enriquecida com fosfato natural, calcário, torta de mamona, etc... A cada 15 dias se faz o reviramento das camadas e umedecendo-as. O produto deve ficar protegido, por plástico ou lona, da chuva e do solo. O composto está pronto quando ele apresentar uma redução de volume de 1/3 e não ser possível distinguir os componentes iniciais. O vermicomposto é um orgânico composto resultante da digestão da matéria orgânica proveniente de estercos, restos vegetais e outros resíduos orgânicos pelas minhocas. O lodo de esgoto é um orgânico composto resultante do tratamento de esgotos sanitários dando origem a um produto de utilização segura na agricultura atendendo aos limites estabelecidos para contaminantes.
4. Organo-minerais – são misturas de fertilizantes minerais com orgânicos simples ou compostos. Não sofrem nenhum tratamento. No caso dos fertilizantes minerais, estes devem ser naturais e de baixa solubilidade. É o caso dos fosfatos naturais, calcário, que são produtos originados de rochas apenas moídas e não sofreram nenhum tratamento químico. O superfosfato simples, fonte de P2O5, não pode ser usado, apesar de a origem ser um fosfato natural, pois é tratado com ácido sulfúrico para aumentar a solubilidade. Apenas com autorização é permitido o uso de termofosfatos que são fosfatos naturais submetidos a um tratamento térmico a temperaturas acima de 1.000 ºC.
Seja uma cultura que exige, conforme recomendação técnica, 150 kg/ha de N, 250 kg/ha de P2O5 e 180 kg/ha de K2O.
Vamos partir do N que contém o esterco bovino. A fórmula a ser usada é:
Qp = Qr x fQp = quantidade de produto em kg/ha
f = 100/%MS
Qp = 150 x 20 = 3.000 kg/ha de esterco bovino
Estes 3.000 kg/ha fornecem em fósforo e potássio, o seguinte:
Fórmula: qdade de nutriente = Qp/f
P2O5 = 3.000/40 = 75 kg/ha
K2O = 3.000/20 = 150 kg/ha
Portanto, o déficit é no fósforo (250 – 75 = 175) e potássio (180 – 150 = 30). Vamos usar o produto cinzas que fornece potássio:
Qp = 30 x 10 = 300 kg/ha de cinzasA cinzas, por sua vez, fornece fósforo:
P2O5 = 300/40 = 7 kg/ha
Até agora, o esterco de bovino e as cinzas forneceram 75+7 = 82 kg/ha de P2O5 O déficit é: 250 – 82 = 168 kg/ha
Utilizemos o fosfato natural:
Qp = 168 x 3,3 = 554 kg/ha
Chegamos ao resultado final de 3.000 kg/ha de esterco bovino; 300 kg/ha de cinzas e 554 kg/ha de fosfato natural.
Leia os outros artigos Parte 1 e Parte 2
Produtos orgânicos x fertilizantes minerais - Parte 1
Produtos orgânicos X fertilizantes minerais - Parte 2
1. Simples – são aqueles originados de plantas ou de animais. É o caso dos estercos de bovinos e suínos, camas de f
 rango, torta de mamona, vermicomposto, turfa, linhita, etc... O esterco fresco, que contém microorganismos causadores de doenças no homem, não é permitido o seu uso em culturas, em que a parte comestível pela população humana possa entrar em contato direto com ele. Para isto, ele deve ser “curtido”, processo que pode levar até 90 dias dependendo das condições climáticas. O esterco fresco, durante o curtimento, deve ficar protegido e ser evitado o escorrimento de água que levaria embora os nutrientes contido neles.
rango, torta de mamona, vermicomposto, turfa, linhita, etc... O esterco fresco, que contém microorganismos causadores de doenças no homem, não é permitido o seu uso em culturas, em que a parte comestível pela população humana possa entrar em contato direto com ele. Para isto, ele deve ser “curtido”, processo que pode levar até 90 dias dependendo das condições climáticas. O esterco fresco, durante o curtimento, deve ficar protegido e ser evitado o escorrimento de água que levaria embora os nutrientes contido neles.2. Mistos – são originados da mistura de dois ou mais orgânicos simples;
3. Compostos – estes não são um orgânico natural. São obtidos por processos químicos, físico, físico-químicos ou biológicos. Podem ser, ainda, enriquecidos com nutrientes minerais. Formados por restos de vegetais e animais são obtidos por via aeróbica (presença de ar). Sua utilização é importante, pois melhora as condições físicas, químicas, físico-químicas e biológicas do solo favorecendo o enraízamento das plantas. Nos compostos se usa restos de vegetais, ricos em carbono (C), e de animais. O esterco é rico em nitrogênio (N). Isto é importante para estabelecer a relação C/N, que inicialmente deve ser 30/1. Devem-se usar mais resíduos vegetais ricos em carbono. O processo para formar o composto é distribuir camadas alternadas de restos vegetais e de animais. Cada camada vai sendo umedecida com água evitando-se o escorrimento para não haver perda de nutrientes. Pode ser enriquecida com fosfato natural, calcário, torta de mamona, etc... A cada 15 dias se faz o reviramento das camadas e umedecendo-as. O produto deve ficar protegido, por plástico ou lona, da chuva e do solo. O composto está pronto quando ele apresentar uma redução de volume de 1/3 e não ser possível distinguir os componentes iniciais. O vermicomposto é um orgânico composto resultante da digestão da matéria orgânica proveniente de estercos, restos vegetais e outros resíduos orgânicos pelas minhocas. O lodo de esgoto é um orgânico composto resultante do tratamento de esgotos sanitários dando origem a um produto de utilização segura na agricultura atendendo aos limites estabelecidos para contaminantes.
4. Organo-minerais – são misturas de fertilizantes minerais com orgânicos simples ou compostos. Não sofrem nenhum tratamento. No caso dos fertilizantes minerais, estes devem ser naturais e de baixa solubilidade. É o caso dos fosfatos naturais, calcário, que são produtos originados de rochas apenas moídas e não sofreram nenhum tratamento químico. O superfosfato simples, fonte de P2O5, não pode ser usado, apesar de a origem ser um fosfato natural, pois é tratado com ácido sulfúrico para aumentar a solubilidade. Apenas com autorização é permitido o uso de termofosfatos que são fosfatos naturais submetidos a um tratamento térmico a temperaturas acima de 1.000 ºC.
Seja uma cultura que exige, conforme recomendação técnica, 150 kg/ha de N, 250 kg/ha de P2O5 e 180 kg/ha de K2O.

Vamos partir do N que contém o esterco bovino. A fórmula a ser usada é:
Qp = Qr x fQp = quantidade de produto em kg/ha
f = 100/%MS
Qp = 150 x 20 = 3.000 kg/ha de esterco bovino
Estes 3.000 kg/ha fornecem em fósforo e potássio, o seguinte:
Fórmula: qdade de nutriente = Qp/f
P2O5 = 3.000/40 = 75 kg/ha
K2O = 3.000/20 = 150 kg/ha
Portanto, o déficit é no fósforo (250 – 75 = 175) e potássio (180 – 150 = 30). Vamos usar o produto cinzas que fornece potássio:
Qp = 30 x 10 = 300 kg/ha de cinzasA cinzas, por sua vez, fornece fósforo:
P2O5 = 300/40 = 7 kg/ha
Até agora, o esterco de bovino e as cinzas forneceram 75+7 = 82 kg/ha de P2O5 O déficit é: 250 – 82 = 168 kg/ha
Utilizemos o fosfato natural:
Qp = 168 x 3,3 = 554 kg/ha
Chegamos ao resultado final de 3.000 kg/ha de esterco bovino; 300 kg/ha de cinzas e 554 kg/ha de fosfato natural.
Leia os outros artigos Parte 1 e Parte 2
Produtos orgânicos x fertilizantes minerais - Parte 1
Produtos orgânicos X fertilizantes minerais - Parte 2
segunda-feira, 18 de maio de 2009
Os Fosfatos perante à Legislação Brasileira
A Legislação Brasileira determina que a garantia do fósforo deve ser avaliada nos seguintes extratores químicos:
• Fosfatos Acidulados e parcialmente Acidulados – Citrato neutro de amônio (CNA) + água, e os teores solúveis em água e total para os parcialmente acidulados quando comercializados isoladamente;
• Misturas que contenham fosfatos acidulados ou parcialmente acidulados – citrato neutro de amônio (CNA) + água e facultativo o teor solúvel em água;
• Fosfato Naturais, Fosfatos Naturais Reativos, Escórias, Termofosfatos e Farinha de Ossos – o teor total de fósforo e o teor solúvel em ácido cítrico a 2% relação 1:100; No caso dos Fosfatos Naturais Reativos pode ser indicada o teor de fósforo solúvel em ácido fórmico a 2% relação 1:100 desde que o teor de fósforo solúvel encontrado neste extrator (ácido fórmico) seja igual ou maior que 55% do fósforo total do produto.
• Misturas que contenham fosfato natural, fosfato natural reativo, escórias e farinha de ossos - teor total de fósforo somente em misturas de natureza física pó ou farelada; fósforo solúvel em ácido cítrico 2% na relação 1:100 e teor de fósforo solúvel em água ou informação de que o fósforo é insolúvel em água;
• Misturas que contenham termofosfatos – teor total somente quando em misturas de natureza física pó ou farelada; teor solúvel de fósforo em ácido cítrico a 2% relação 1:100 ou teor de fósforo solúvel em citrato neutro de amônio (CNA) + água.
O fósforo é avaliado na forma de P2O5. No caso do ácido cítrico a 2%, a relação 1:100, quer dizer 1 gramo de produto para 100 ml de ácido. Um avanço da Legislação de Fertilizantes foi permitir a indicação da solubilidade em ácido fórmico 2% 1:100 para os fosfatos naturais reativos. Isto era uma antiga aspiração dos que defendiam os fosfatos naturais reativos.
• Fosfatos Acidulados e parcialmente Acidulados – Citrato neutro de amônio (CNA) + água, e os teores solúveis em água e total para os parcialmente acidulados quando comercializados isoladamente;
• Misturas que contenham fosfatos acidulados ou parcialmente acidulados – citrato neutro de amônio (CNA) + água e facultativo o teor solúvel em água;
• Fosfato Naturais, Fosfatos Naturais Reativos, Escórias, Termofosfatos e Farinha de Ossos – o teor total de fósforo e o teor solúvel em ácido cítrico a 2% relação 1:100; No caso dos Fosfatos Naturais Reativos pode ser indicada o teor de fósforo solúvel em ácido fórmico a 2% relação 1:100 desde que o teor de fósforo solúvel encontrado neste extrator (ácido fórmico) seja igual ou maior que 55% do fósforo total do produto.
• Misturas que contenham fosfato natural, fosfato natural reativo, escórias e farinha de ossos - teor total de fósforo somente em misturas de natureza física pó ou farelada; fósforo solúvel em ácido cítrico 2% na relação 1:100 e teor de fósforo solúvel em água ou informação de que o fósforo é insolúvel em água;
• Misturas que contenham termofosfatos – teor total somente quando em misturas de natureza física pó ou farelada; teor solúvel de fósforo em ácido cítrico a 2% relação 1:100 ou teor de fósforo solúvel em citrato neutro de amônio (CNA) + água.
O fósforo é avaliado na forma de P2O5. No caso do ácido cítrico a 2%, a relação 1:100, quer dizer 1 gramo de produto para 100 ml de ácido. Um avanço da Legislação de Fertilizantes foi permitir a indicação da solubilidade em ácido fórmico 2% 1:100 para os fosfatos naturais reativos. Isto era uma antiga aspiração dos que defendiam os fosfatos naturais reativos.

O mercado comum europeu utiliza o ácido fórmico há anos pois dizem que é o único extrator para diferenciar os fosfatos naturais reativos dos fosfatos de baixa reatividade desde que 55% do seu fósforo total seja solúvel no ácido fórmico 2% 1:100. E estão corretos pois pesquisas realizadas no Brasil confirmam este fato, como vejamos: dos fosfatos naturais, na ilustração acima, o único que poderia ser comercializado no Mercado Comum Europeu seria o fosfato natural de Gafsa – pois no teste realizado por Catani e Nascimento, 94,6% do fósforo total do Gafsa é solúvel no ácido fórmico 2% 1:100. Os fosfatos naturais brasileiros são de baixa reatividade e não servem para aplicação direta na agricultura mas podem ser utilizados pelas indústrias onde sofrerão tratamentos químicos que os tornarão solúveis em água.
terça-feira, 5 de maio de 2009
O Ciclo dos Fosfatos Naturais
Os fosfatos naturais reativos, sedimentares, amorfos e micropulverizados podem ser aplicados diretamente no solo pois apresentam uma eficiência agronômica muito boa. Para ser um fosfato reativo deve ter no mínimo 55% do seu fósforo total solúvel no ácido fórmico 2% relação 1:100.
No solo, os fosfatos naturais reativos apresentam o seguinte ciclo:
- o fósforo (P) do fosfato natural reativo encontra-se na forma tricálcica é solubilizado de modo imediato, progressivo e constante, permitindo às plantas uma disponibilidade permanente de fósforo nas quantidades necessárias e durante todo o ciclo da planta. Nos fosfatos acidulados ou solúveis em água (supersimples e supertriplo) a disponibilidade do fósforo é total e por um curto período. Em 1989, o departamento químico da extinta Companhia Riograndense de Adubos - CRA, sob a liderança do Eng° Químico F. Mottola realizou um teste com o HIPERFOSFATO (fosfato natural de alta reatividade, importado da África do Norte - GAFSA) tratando um gramo do produto com ácido cítrico a 2% 1:300 e a quantidade de fósforo extraída foi 12%. Trataram novamente o resíduo com o mesmo extrator e, novamente, obteram 12% e assim sucessivamente. Com os fosfatos naturais brasileiros obteram na 1a. extração 6 -7% e nas seguintes praticamente nada de fósforo. Nos fosfatos naturais reativos a solubilidade, no solo, é realizada: pela acidez livre do solo (H+); ação dos ácidos orgânicos sintetizados pelos microorganismos na mineralização da matéria orgânica; pelas secreções ácidas das raízes. Nas pontas das raízes exite sempre uma zona ácida que provoca a solubilização do fósforo do fosfato natural reativo; ação do CO2 do ar do solo; quando sofrem um rigoroso processo de moagem ou seja, moídos a um grau elevado de finura e devido a sua natureza branda, os fosfatos naturais altamente reativos não tem similar; Ocorre, também, o processo de fixação, mas bem menor que àquele sofrido pelos fosfatos solúveis em água, pois as quantidades disponíveis de fósforo são bem menores durante um mesmo período. A solubilização dos fosfatos naturais altamente reativos é constante;
- parte do fósforo disponível é absorvida pelas plantas e outra pelos microorganismos (fósforo imobilizado);
- a pequena parte do fósforo fixado voltará a tornar-se disponível pela ação dos ácidos orgânicos do solo, pela acidez livre (H+), pelas secreções ácidas das raízes e pelo CO2 do ar do solo;
- o fósforo imobilizado pode tornar-se novamente disponível pela mineralização da matéria orgânica.
Compare os ciclos dos fosfatos acidulados (texto já postado) com este dos fosfatos naturais reativos. Quando indico fosfatos naturais para serem aplicados diretamente na agricultura refiro-me aos REATIVOS.
sábado, 2 de maio de 2009
Os Fosfatos Naturais
Existem fosfatos que são insolúveis em água mas que podem ser utilizados diretamente para aplicação no solo. São os fosfatos naturais que não sofrem nenhum tratamento químico ou térmico. Mas atenção: nem todo fosfato natural serve para aplicação direta no solo. Somente os fosfatos naturais que apresentam alta solubilidade em ácido fórmico são os mais reativos. Porque na Europa o ácido fórmico 2% relação 1:100 é considerado o melhor extrator para avaliar a eficiência de um fosfato natural. Durante o século XIX, muitos químicos e engenheiros-agrônomos acreditavam que somente o fósforo solúvel em água era assimilado pelas plantas. Até a década de 70 este conceito errôneo era ainda praticado pois aprendia-se, nos bancos das Universidades, que o fosfato natural servia somente para ser atacado por ácidos (sulfúrico e fosfórico) e obtinham-se os superfosfatos simples e triplo. As legislações de fertilizantes da época contribuiram, também, para desvalorizar os fosfatos naturais. O solo como meio vivo, dinâmico, era esquecido. Apesar de insolúvel em água, o P2O5 contido nos fosfatos naturais pode ser utilizado pelas plantas devido aos seguintes fenômenos:
- dissolução no solo dos fosfatos naturais por soluções ácidas que reagem da mesma maneira que os ácidos sulfúrico, fosfórico utilizados pelas indústrias. O ácido cítrico presente no solo faria o mesmo papel;
- sua absorção pelo solo, acelera o ciclo do fósforo;
- ataque e absorção direta pelas raízes que segregam substâncias ácidas que são capazes de tornar solúvel as partículas de fosfatos que entram em contato com elas.
Entretanto, para que o fósforo contido nos fosfatos naturais tenha, virtualmente, o mesmo efeito ou o mais aproximado do fósforo solúvel em água é necessário duas condições importantes:
1. Utilização de fosfatos brandos de origem orgânica e sedimentar (amorfos) – isto é de grande reatividade agronômica. Não ocorrendo isto, a ação do fosfato natural será tão lenta e, praticamente nula;
2. Micropulverização destes fosfatos de forma a aumentar a área de superfície das partículas aumentando assim, ao máximo, o contato entre os ácidos do solo e o fosfato.
A solubilidade do fósforo contido nos diversos fosfatos é avaliada por diversos extratores químicos tais como: ácido cítrico, citrato, água + citrato, ácido fórmico. Estes processos apenas estimam a solubilidade do fósforo, declarado no fertilizante, enquanto no solo ocorrem processos de solubilização ainda desconhecidos pela ciência.
Segundo algumas pesquisas, "não há relação entre a solubilidade avaliada por extratores químicos e a eficiência agronômica" (Macedo-W.S.L - Resposta à aplicação de calcário e diferentes fontes de fósforo em misturas forrageiras, em dois tipos de solo. Tese -Faculdade de Agronomia -UFRGS - Porto Alegre - maio/1975). O fosfato natural apesar de ser insolúvel em água, sofre no solo, um processo de solubilização similar ao industrial quando é atacado por ácidos (sulfúrico, cítrico, fósforico e orgânicos) ou, então, é solubilizado por substâncias secretadas nas zonas das raízes. Graças à situação que o solo é um meio dinâmico, que não serve apenas para fixar a planta, mas é um meio vivo com propriedades bioquímicas aliadas às da planta, à pobreza de fósforo, na maioria dos solos cultivados, tem-se observado a eficiência agronômica dos fosfatos naturais de alta reatividade, nas mais diferentes partes do mundo e em diversas pesquisas.
Em solos ácidos, como é o caso do Brasil, onde o fósforo é fortemente fixado quando aplicado na forma solúvel em água, explica-se porque os fosfatos naturais reativos apresentam respostas favoráveis quando aplicados no solo.
Segundo algumas pesquisas, "não há relação entre a solubilidade avaliada por extratores químicos e a eficiência agronômica" (Macedo-W.S.L - Resposta à aplicação de calcário e diferentes fontes de fósforo em misturas forrageiras, em dois tipos de solo. Tese -Faculdade de Agronomia -UFRGS - Porto Alegre - maio/1975). O fosfato natural apesar de ser insolúvel em água, sofre no solo, um processo de solubilização similar ao industrial quando é atacado por ácidos (sulfúrico, cítrico, fósforico e orgânicos) ou, então, é solubilizado por substâncias secretadas nas zonas das raízes. Graças à situação que o solo é um meio dinâmico, que não serve apenas para fixar a planta, mas é um meio vivo com propriedades bioquímicas aliadas às da planta, à pobreza de fósforo, na maioria dos solos cultivados, tem-se observado a eficiência agronômica dos fosfatos naturais de alta reatividade, nas mais diferentes partes do mundo e em diversas pesquisas.
Em solos ácidos, como é o caso do Brasil, onde o fósforo é fortemente fixado quando aplicado na forma solúvel em água, explica-se porque os fosfatos naturais reativos apresentam respostas favoráveis quando aplicados no solo.
Por volta dos anos 70, a legislação estabelecia que a solubilidade dos fosfatos naturais seria determinada no extrator ácido citríco 2% relação 1:300. Um fosfato de alta reatividade, originário da África do Norte, região de Gafsa, era comercializado com os teores de 30% de P2O5 total e 24% de P2O5 solúvel no ácido cítrico a 2% relação 1:300. A relação 1:300 significa uma grama de fosfato e 300 ml de ácido. Por interesses comerciais, a Legislação alterou a relação para 1:100. Nesta relação a solubilidade do Fosfato de Gafsa caiu para 12%. O produto, por um artifício da legislação, foi desvalorizado. Os extratores não são universais.
Na Europa se usa o ácido fórmico 2% 1:100 como extrator e é exigido que 55% do fósforo total seja solúvel neste ácido, para considerar um fosfato natural reativo (FNR). Para os europeus, o ácido fórmico é o melhor extrator para diferenciar fosfatos naturais reativos, de alta eficiência agronômica, dos fosfatos não reativos, de baixa eficiência. Nos Estados Unidos, utilizam o citrato neutro de amônio.
Portantos temos rochas fosfatados de baixa eficiência que não podem ser utilizadas diretamente na agricultura e precisam sofrer o processo de acidulação (tratamento por ácidos) e encontramos rochas fosfatadas reativas que podem ser usadas diretamente na agricultura pela sua grande eficiência agronômica desde que sejam amorfas e micropulverizadas. Os fosfatos naturais reativos são os de Gafsa, Carolina do Norte, Arad.
A última atualização da Legislação Brasileira, em vigor, veio valorizar os fosfatos naturais reativos permitindo que seja expresso pelo seu teor em P2O5 solúvel no ácido fórmico 2% 1:100 desde que represente, no mínimo, 55% do teor de fósforo total.
Assinar:
Postagens (Atom)